БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ - Е. С. Северина - 2004
РАЗДЕЛ 7. ОБМЕН УГЛЕВОДОВ
X. Регуляция гликолиза и глюконеогенеза в печени
По сравнению с другими органами печень отличается наиболее сложным обменом глюкозы. Кроме пары противоположных процессов (синтеза и распада гликогена), в печени могут происходить ещё два противоположно направленных процесса — гликолиз и глюконеогенез. В большинстве других органов происходит только гликолиз. Переключение печени с гликолиза на глюконеогенез и обратно происходит с участием инсулина и глюкагона и осуществляется с помощью:
✵ аллостерической регуляции активности ферментов;
✵ ковалентной модификации ферментов путём фосфорилирования/дефосфорилирования;
✵ индукции/репрессии синтеза ключевых ферментов.
Регуляторные воздействия направлены на ферменты, катализирующие необратимые стадии гликолиза и глюконеогенеза, сочетание которых называют «субстратными», или «холостыми» циклами.
А. Регуляция скорости реакций гликолиза и глюконеогенеза, составляющих субстратные циклы
«Субстратные» циклы — парные комбинации процессов синтеза и распада метаболитов. Как уже упоминалось, сочетание процессов синтеза и распада гликогена или необратимых реакций гликолиза и соответствующих им необратимых реакций глюконеогенеза может составить подобный цикл. Название «субстратный цикл» означает объединение реакций синтеза и распада субстрата. Название «холостой» отражает результат работы подобного цикла, заключающийся в бесполезном расходовании АТФ. Хотя существование «холостых» циклов нелогично, тем не менее они могут функционировать. Более того, эти циклы могут быть мишенью регуляторных воздействий, так как составляющие их реакции катализируют разные ферменты. Реципрокное изменение активности этих ферментов предотвращает одновременное протекание противоположных процессов.
Изменение в печени гликолитического направления на глюконеогенез и обратно при смене абсорбтивного состояния на постабсорбтивное или при голодании происходит главным образом в результате регуляции активности ферментов, катализирующих реакции субстратных циклов. Эти циклы обозначены цифрами I, II, III на рис. 7-54, представляющем общую картину регуляции гликолиза и глюконеогенеза в печени.
Рис. 7-54. Регуляция метаболизма глюкозы в печени. БИФ — бифункциональный фермент (фруктозо-2,6-бисфосфатаза/фосфофруктокиназа-2); БИФ-ОН — дефосфорилированный фермент; БИФ-Р — фосфорилированный фермент, ПДК-ОН — дефосфорилированный пируватдегидрогеназный комплекс; ПК-ОН — дефосфорилированная пируваткиназа; ГАФ — глицеральдегидфосфат; ДАФ — дигидроксиацетонфосфат, ФЕП — фосфоенолпируват. I-III — субстратные циклы: в рамках — регуляторные ферменты глиполиза и глюконеогенеза.

Направление реакции первого субстратного цикла регулируется главным образом концентрацией глюкозы. При пищеварении концентрация глюкозы в крови повышается (до 8— 10 ммоль/л). Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется гликолитическая реакция образования глюкозо-6-фосфата. Кроме того, инсулин индуцирует синтез глюкокиназы и ускоряет тем самым фосфорилирование глюкозы. Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата в абсорбтивном периоде направляется на синтез гликогена и по гликолитическому пути.
Направление реакций второго субстратного цикла зависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата. Активность этих ферментов зависит от концентрации фруктозо-2,6-бисфосфата. Фруктозо-2,6-бисфосфат — метаболит, образующийся в незначительных количествах из фруктозо-6-фосфата и выполняющий только регуляторные функции. Образование фруктозо-2,6-бисфосфата путём фосфорилирования фруктозо-6-фосфата катализирует бифункциональный фермент (БИФ),который катализирует также и обратную реакцию (рис. 7-55, А). Однако превращение фрукгозо-2,6-бисфосфата в фруктозо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6-бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата гидролитически отщепляется неорганический фосфат.
Рис. 7-55. Реакции, катализируемые бифункциональным ферментом (БИФ) в печени (А). Регуляция активности БИФ (Б).

В реакции фосфорилирования фруктозо-6- фосфата фермент проявляет киназную активность, а при дефосфорилировании образованного фруктозо-2,6-бисфосфата — фосфатазную. Это обстоятельство и определило название фермента «бифункциональный».
Киназная активность БИФ проявляется, когда фермент находится в дефосфорилированной форме (БИФ-ОН). Дефосфорилированная форма БИФ характерна для абсорбтивного периода, когда инсулин/глюкагоновый индекс высокий. В этот период количество фруктозо-2,6-бисфосфата увеличивается (рис. 7-55, Б).
При низком инсулин-глюкагоновом индексе, характерном для периода длительного голодания, происходит фосфорилирование БИФ, и он функционирует как фосфатаза. Результат — снижение количества фруктозо-2,6-бисфосфата.
Киназную и фосфатазную реакции катализируют разные активные центры БИФ, но в каждом из двух состояний фермента (фосфорилированном и дефосфорилированном) один из активных центров ингибирован. Регуляторное влияние фруктозо-2,6-бисфосфата заключается в том, что он аллостерически активирует фосфофруктокиназу (фермент гликолиза). При этом фруктозо-2,6-бисфосфат снижает ингибирующее действие АТФ на этот фермент в абсорбтивном периоде и повышает его сродство к фруктозо-6- фосфату. В то же время фруктозо-2,6-бисфосфат ингибирует фруктозо-1,6-бисфосфатазу (фермент глюконеогенеза). Итак, в абсорбтивном периоде уровень фруктозо-2,6-бисфосфата повышается, что приводит к активации фосфофруктокиназы и ускорению гликолиза.
Результатом уменьшения количества фрукто- зо-2,6-бисфосфата в постабсорбтивном периоде будет снижение активности фосфофруктокиназы, замедление гликолиза и переключение гликолиза на глюконеогенез. Регуляторное влияние фруктозо-2,6-бисфосфата представлено на рис. 7-56.
Рис. 7-56. Регуляция реакций II субстратного цикла фруктозо-2,6-бисфосфатом.

В регуляции третьего субстратного цикла основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная — активна (рис. 7-57).
Рис. 7-57. Регуляция пируваткиназы в печени.

В период пищеварения инсулин активирует фосфопротеинфосфатазу, которая дефосфорилирует пируваткиназу, переводя её в активное состояние. Кроме того, инсулин в печени влияет на количество ферментов, индуцируя синтез пиру- ваткиназы и репрессируя синтез фосфоенолпируваткарбоксикиназы. Следовательно, гликолитическая реакция фосфоенолпируват —> пируват ускоряется при пищеварении. Эта же реакция замедляется в постабсорбтивном состоянии под влиянием глюкагона, который опосредованно через цАМФ-зависимую протеинкиназу фосфорилирует и инактивирует пируваткиназу.
При длительном голодании глюкагон ускоряет глюконеогенез. Это достигается не только путём фосфорилирования пируваткиназы и снижением скорости гликолиза, но и путём индукции синтеза ферментов глюконеогенеза: фосфоенолпируваткарбоксикиназы, фруктозо- 1,6-бисфосфатазы и глюкозо-6-фосфатазы. Известно, что глюкагон, фосфорилируя опосредованно транскрипционные факторы, влияет на их активность и таким образом индуцирует синтез этих ферментов глюконеогенеза. Кроме того, синтез фосфоенолпируваткарбоксикиназы при длительном голодании индуцируется кортизолом, однако это происходит в результате включения другого механизма действия, характерного для стероидных гормонов (см. разделы 5, 11).
Координация скорости реакции II и III субстратных циклов достигается с помощью фруктозо-1,6-бисфосфата — продукта II субстратного цикла (гликолитическое направление), который является аллостерическим активатором пируваткиназы. В период пищеварения вследствие ускорения начальных стадий гликолиза концентрация фруктозо-1,6-бисфосфата повышается, что приводит к дополнительной активации пируваткиназы.
Общая картина регуляции процессов, составляющих метаболизм глюкозы в печени, представлена на рис. 7-54.
Необходимо отметить, что противоположные реакции каждого из субстратных циклов могут протекать одновременно. Соответственно, гликолиз и глюконеогенез в печени в какой-то мере тоже могут происходить одновременно, хотя их относительные скорости изменяются. Так, при пищеварении преобладает гликолитическое направление, а в постабсорбтивном состоянии — направление глюконеогенеза. Например, реакция глюконеогенеза пируват —> оксалоацетат может протекать при любых состояниях организма. Это объясняется необходимостью поддерживать концентрацию оксалоацетата на определённом уровне, потому что оксалоацетат используется не только в глюконеогенезе, но и в других процессах, таких как цитратный цикл, трансмембранный перенос веществ, синтез аминокислот.
Б. Значение гликолиза в печени для синтеза жиров
Основным значением ускорения гликолиза в печени в период пищеварения является образование дигидроксиацетонфосфата и ацетил-КоА — исходных веществ для синтеза жира. Образование ацетил-КоА из пирувата в ходе реакции, катализируемой ПДК, регулируется разными способами и подробно описывалось в разделе 6.
В абсорбтивном периоде ПДК находится в дефосфорилированной (активной) форме, следовательно, декарбоксилирование пирувата ускоряется. Образуемый ацетил-КоА используется в основном двумя путями: для синтеза жирных кислот и в цитратном цикле. В период пищеварения ускоряются образование ацетил-КоА и его использование для синтеза жирных кислот. Необходимый для синтеза жира α-глицерофосфат образуется в реакции восстановления из дигидроксиацетонфосфата (рис. 7-58). Подробно этот процесс рассматривается в разделе 8.
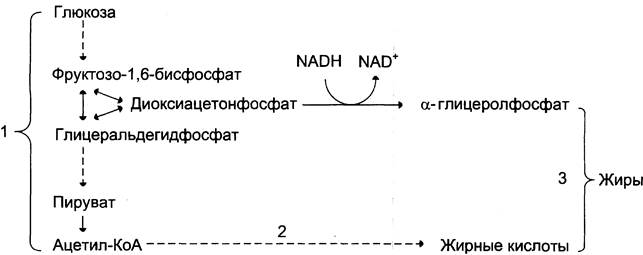
Рис. 7-58. Синтез жира из углеводов. 1 — окисление глюкозы до пирувата и окислительное декарбоксилирование пирувата приводят к образованию ацетил-КоА; 2 — ацетил-КоА является строительным блоком для синтеза жирных кислот; 3 — жирные кислоты и α-глицеролфосфат, образующийся в реакции восстановления дигидроксиацетонфосфата, участвуют в синтезе триацилглицеролов.
В. Аллостерическая регуляция аэробного распада глюкозы и глюконеогенеза в печени энергетическим статусом клетки
Аллостерическая регуляция скорости гликолиза, зависимая от изменения соотношения АТФ/АДФ, направлена на изменение скорости использования глюкозы непосредственно клетками печени. Глюкоза в клетках печени используется не только для синтеза гликогена и жиров, но также и как источник энергии для синтеза АТФ. Основными потребителями АТФ в гепатоцитах являются процессы трансмембранного переноса веществ, синтез белков, гликогена, жиров, глюконеогенез. От скорости утилизации АТФ в этих процессах зависит скорость его синтеза. АТФ, АДФ и АМФ, а также NAD+ и NADH служат аллостерическими эффекторами некоторых гликолитических ферментов и ферментов глюконеогенеза. В частности, АМФ активирует фосфофруктокиназу и ингибирует фруктозо-1,6- бисфосфатазу. АТФ и NADH ингибируют пируваткиназу, а АДФ ингибирует пируваткарбоксилазу.
Следовательно, при усилении расходования АТФ и снижении его концентрации с одновременным увеличением концентрации АМФ, активируется гликолиз и образование АТФ, а глюконеогенез при этом замедляется. Кроме того, от соотношения АТФ/АДФ, АМФ и NAD/ NADH зависит скорость реакций общего пути катаболизма (см. раздел 6).