БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ - Е. С. Северина - 2004
РАЗДЕЛ 9. ОБМЕН И ФУНКЦИИ АМИНОКИСЛОТ
VII. Биосинтез заменимых аминокислот
В организме человека возможен синтез восьми заменимых аминокислот: Ала, Асп, Асн, Сер, Гли, Глу, Глн, Про (рис. 9-23). Углеродный скелет этих аминокислот образуется из глюкозы, α-Аминогруппа вводится в соответствующие α- кетокислоты в результате реакций трансамини- рования. Универсальным донором α-аминогруппы служит глутамат.
Рис. 9-23. Пути биосинтеза заменимых аминокислот.

Путём трансаминирования α-кетокислот, образующихся из глюкозы, синтезируются аминокислоты (см. схему А).

Глутамат также образуется при восстановительном аминировании α-кетоглутарата глутаматдегидрогеназой.
Эти реакции обратимы и играют большую роль как в процессе синтеза аминокислот, так и при их катаболизме. Такие реакции, выполняющие двойную функцию, называют амфиболическими.
Амиды глутамин и аспарагин синтезируются из соответствующих дикарбоновых аминокислот Глу и Асп (см. схему А).
✵ Серин образуется из 3-фосфоглицерата — промежуточного продукта гликолиза, который окисляется до 3-фосфопирувата и затем трансаминируется с образованием серина (см. схему Б).

✵ Существует 2 пути синтеза глицина:
1) из серина с участием производного фолиевой кислоты в результате действия сериноксиметилтрансферазы:

2) в результате действия фермента глицин- синтазы в реакции:

✵ Пролин синтезируется из глутамата в цепи обратимых реакций. Эти же реакции используются и при катаболизме пролина (см. схему).
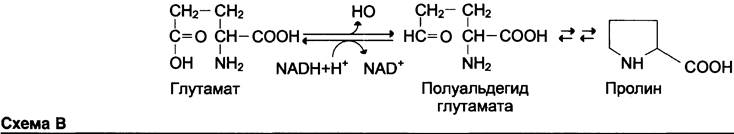
Кроме восьми перечисленных заменимых аминокислот, в организме человека могут синтезироваться ещё четыре аминокислоты.
Частично заменимые аминокислоты Apг и Гис синтезируются сложным путём в небольших количествах. Большая их часть должна поступать с пищей.
✵ Синтез аргинина происходит в реакциях ор- нитинового цикла (см. выше подраздел TV);
✵ Гистидин синтезируется из АТФ и рибозы. Часть имидазольного цикла гистидина -N = CH-NH- образуется из пуринового ядра аденина, источником которого служит АТФ, остальная часть молекулы — из атомов рибозы. При этом образуется 5-фосфорибозиламин, который кроме синтеза гистидина необходим для синтеза пуринов.

Для синтеза условно заменимых аминокислот тирозина и цистеина требуются незаменимые аминокислоты фенилаланин и метионин соответственно (см. подразделы VIII и IX).
Образование других аминокислот также возможно при наличии соответствующих α-кетокислот, которые могут трансаминироваться с глутаматом. Таким образом, незаменимой частью молекулы аминокислот является их углеродный скелет. Источником таких незаменимых α-кето- кислот служат только белки пищи. Исключение составляют лизин и треонин, которые не подвергаются трансаминированию, их α-кетоаналоги с пищей практически не поступают и в организме не синтезируются. Единственный источник этих аминокислот — пищевые белки.